NộI Dung
Để đơn giản là tính toán của họ, các nhà hóa học đã tạo ra một đơn vị tiêu chuẩn cho số lượng nguyên tử của một hợp chất cụ thể liên quan đến một phản ứng hoặc một số quá trình hóa học khác. Họ định nghĩa một mol (mol) là số lượng của bất kỳ chất nào có cùng số đơn vị cơ bản là 12 gram carbon-12, đó là số Avogadros (6.022 × 1023). Hệ thống đo lường SI (hệ mét) xác định một milimol (Mmol) là một phần nghìn của một nốt ruồi. Bạn thường tính số mol của một chất bằng cách cân số lượng bạn có trong tay. Nếu bạn muốn chuyển đổi thành Mmol, nhân với 103 (1,000).
TL; DR (Quá dài; Không đọc)
Một nốt ruồi bằng số hạt Avogadros của một hợp chất cụ thể. Một millimole (Mmol) là một phần nghìn của một nốt ruồi.
Cách tính nốt ruồi
Khối lượng nguyên tử được đo bằng đơn vị khối lượng nguyên tử (AMU). Một AMU chính xác bằng 1/12 khối lượng hạt nhân của nguyên tử carbon-12 ở trạng thái cơ bản. Một mol của một chất được xác định bằng với số hạt Avogadros của chất đó. Theo định nghĩa này, trọng lượng của một mol của một chất tính bằng gam là số tương đương với trọng lượng của một hạt riêng lẻ của chất đó trong AMU. Ví dụ, trọng lượng nguyên tử của carbon-12 là 12 AMU, do đó, một mol carbon-12 nặng 12 gram.
Hãy xem xét một thùng chứa đầy khí hydro (H2). Mỗi hạt trong vật chứa là một phân tử gồm hai nguyên tử hydro, vì vậy bạn chỉ cần biết khối lượng nguyên tử của hydro để tính trọng lượng phân tử. Hầu hết các phiên bản của bảng tuần hoàn liệt kê khối lượng nguyên tử của mỗi nguyên tố dưới ký hiệu của nó. Đối với hydro, có một proton duy nhất trong hạt nhân, 1,008 AMU của nó, là trung bình của tất cả các đồng vị xuất hiện tự nhiên của hydro. Do đó, khối lượng nguyên tử của khí hydro là 2.016 AMU và một mol khí hydro nặng 2.016 gram. Để tìm số mol trong mẫu của bạn, bạn sẽ cân mẫu bằng gam và chia trọng lượng đó cho trọng lượng phân tử của khí hydro tính bằng gam. Ví dụ, một mẫu nặng 15 gram khí hydro tinh khiết chứa 7,44 mol.
Chuyển đổi sang Mmol
Đôi khi số lượng được điều tra quá nhỏ đến nỗi việc thể hiện chúng trong nốt ruồi là cồng kềnh. Nhập millimole. Bằng cách nhân số mol với một nghìn, bạn có thể chuyển đổi một số rất nhỏ thành một số dễ quản lý hơn. Điều này đặc biệt thuận tiện khi xử lý các đơn vị khối lượng theo thứ tự mililít.
1 mol = 1.000 mol
Dung dịch cô đặc
Các nhà hóa học sử dụng nồng độ mol như một thước đo nồng độ của một hợp chất cụ thể trong dung dịch. Họ định nghĩa số mol là số mol mỗi lít. Bạn chuyển đổi số mol thành millimole bằng cách nhân với 1.000. Ví dụ, dung dịch 1 mol (mol, cũng được viết là M) có nồng độ 1 mol mỗi lít. Điều này tương đương với giải pháp 1.000 Mmol (millimole, đôi khi được viết là mM), là giải pháp chứa 1.000 Mmol mỗi lít.
Thí dụ
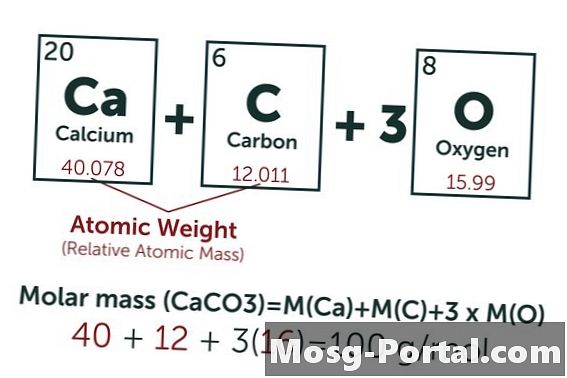
Một dung dịch chứa 0,15 gam canxi cacbonat. Có bao nhiêu millimole?
Công thức hóa học của canxi cacbonat là CaCO3. Trọng lượng nguyên tử của carbon (C) là khoảng 12 AMU, của oxy (O) khoảng 16 AMU và canxi (Ca) khoảng 40 AMU. Mỗi phân tử canxi cacbonat do đó nặng 100 AMU, có nghĩa là một mol nặng khoảng 100 gram. Trọng lượng 0,15 gam tương ứng 0,15 g 100 g / mol = 0,0015 mol. Điều này tương đương với 1,5 Mmol.
Nồng độ mol và milimet của canxi cacbonat này trong 2,5 lít dung dịch là bao nhiêu?
Số mol được định nghĩa là số mol trên một lít, vì vậy hãy chia số mol cho 2,5 để có số mol: 0,0015 2,5 =
0,0006 M
Nhân với 1.000 để có được millimolarity =
0,6 mM
Lưu ý rằng bạn đến cùng một kết quả cho milimol nếu bạn chia số milimol cho thể tích dung dịch.