NộI Dung
Các nhà khoa học dựa vào chuẩn độ trực tiếp để tìm ra lượng chất trong dung dịch có phản ứng hóa học. Khi được thực hiện chính xác, quá trình này có thể mô tả rất chính xác lượng hóa chất bằng cách sử dụng axit chuyên dụng và dụng cụ thủy tinh trong phòng thí nghiệm. Để chuẩn độ hoạt động đúng, phức hợp cuối cùng phải hình thành đủ nhanh để các nhà khoa học phân tích nó.
Định nghĩa
Chuẩn độ trực tiếp là một cách để xác định hàm lượng của một chất định lượng. Các nhà khoa học có thể biết về chất phản ứng, nhưng không biết số lượng chất phản ứng. Chuẩn độ trực tiếp đôi khi dựa trên các chỉ số đáp ứng với vật liệu được phân tích, được gọi là chất phân tích. Những lần khác, các phương pháp dựa trên việc sử dụng các ion kim loại được thêm vào, đó là các nguyên tử hoặc phân tử riêng lẻ của một loại kim loại cụ thể.
Axit ethylenediaminetetracetic và phương pháp đo điện thế
Kỹ thuật viên có thể thực hiện chuẩn độ bằng axit ethylenediaminetetracetic với các chỉ thị ion kim loại. Phương pháp này không hoạt động trong tất cả các tình huống, vì phản ứng đôi khi chậm đến mức việc chuẩn độ trở nên không thực tế. Các ion kim loại đã sử dụng phải có độ ổn định kém hơn chất phân tích. Một phương pháp chuẩn độ trực tiếp khác là phương pháp chiết áp, được sử dụng để phát hiện điểm cuối với các ion kim loại có điện cực cụ thể. Điểm cuối là điểm kết thúc quá trình chuẩn độ.
Chuẩn độ phức
Để chuẩn độ phức tạp, các nhà khoa học sử dụng axit aminopolycarboxylic để xác định kim loại. Các phức màu được hình thành và các nhà khoa học sử dụng dữ liệu thu thập được từ sự hình thành này để xác định số lượng chất phân tích. Phương pháp trực tiếp chuẩn độ phức tạp liên quan đến việc sử dụng dung dịch muối kim loại được chuẩn độ bằng dung dịch phức hợp. Các dung dịch phức hợp chứa các nguyên tử hoặc hợp chất tạo thành phức chất với các nguyên tử hoặc hợp chất khác. Các nhà khoa học tìm thấy điểm tương đương từ một chỉ số được thêm vào. Điểm tương đương là khi chất chuẩn độ được thêm vào bằng cân bằng hóa học với chất phân tích. Stoichiometry liên quan đến phản ứng cân bằng hóa học.
Giải pháp Burette
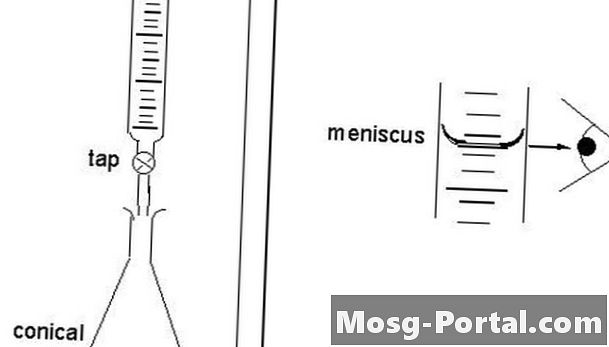
Chuẩn độ trực tiếp được gọi là trực tiếp trực tiếp vì nhà khoa học tiếp cận trực tiếp điểm cuối. Chất chuẩn độ đi vào dung dịch thông qua các giọt từ buret để giọt cuối cùng không vượt qua điểm cuối. Với phương pháp chuẩn độ trực tiếp, các nhà khoa học xử lý một chất hòa tan có trong dung dịch, được chứa trong một bình gọi là chuẩn độ. Dung dịch chuẩn hóa được gọi là chất chuẩn độ. Điểm cuối được xác định bằng phương tiện hoặc trực quan với sự trợ giúp của chỉ báo. Các nhà khoa học thêm chất chuẩn độ vào buret chính xác, một mảnh thủy tinh thẳng đứng và hình trụ với một vòi chính xác giải phóng một lượng nhỏ chất lỏng với số lượng cụ thể. Các nhà khoa học điền vào buret đến 30 đến 100 phần trăm công suất.