NộI Dung
Enzyme là các phân tử protein quan trọng trong các hệ thống sống, sau khi được tổng hợp, thường không được chuyển hóa thành một số loại phân tử khác, cũng như các chất được sử dụng làm nhiên liệu cho các quá trình tiêu hóa và hô hấp (ví dụ, đường, chất béo, oxy phân tử). Điều này là do các enzyme chất xúc tác, điều đó có nghĩa là họ có thể tham gia vào các phản ứng hóa học mà không bị thay đổi, giống như người điều hành cuộc tranh luận công khai, người lý tưởng đưa người tham gia và khán giả đi đến kết luận bằng cách đưa ra các điều khoản của tranh luận trong khi không thêm bất kỳ thông tin độc đáo nào.
Hơn 2.000 enzyme đã được xác định, và mỗi trong số chúng có liên quan đến một phản ứng hóa học cụ thể. Enzyme do đó là đặc trưng cơ chất. Họ được nhóm thành một nửa tá các lớp học trên cơ sở các loại phản ứng mà họ tham gia.
Khái niệm cơ bản về enzyme
Enzyme cho phép một số lượng lớn các phản ứng diễn ra trong cơ thể trong điều kiện cân bằng nội môihoặc cân bằng sinh hóa tổng thể. Ví dụ, nhiều enzyme hoạt động tốt nhất ở mức độ pH (độ axit) gần với độ pH mà cơ thể thường duy trì, nằm trong phạm vi 7 (nghĩa là không có tính kiềm hay axit). Các enzyme khác hoạt động tốt nhất ở pH thấp (độ axit cao) do nhu cầu của môi trường; ví dụ, bên trong dạ dày, nơi một số enzyme tiêu hóa hoạt động, có tính axit cao.
Enzyme tham gia vào các quá trình từ đông máu đến tổng hợp DNA đến tiêu hóa. Một số chỉ được tìm thấy trong các tế bào và tham gia vào các quá trình liên quan đến các phân tử nhỏ, chẳng hạn như glycolysis; một số khác được tiết trực tiếp vào ruột và tác động lên vật chất lớn như thức ăn bị nuốt.
Bởi vì enzyme là protein có khối lượng phân tử khá cao, mỗi loại có hình dạng ba chiều riêng biệt. Điều này xác định các phân tử cụ thể mà họ hành động. Ngoài việc phụ thuộc vào pH, hình dạng của hầu hết các enzyme phụ thuộc vào nhiệt độ, có nghĩa là chúng hoạt động tốt nhất trong một phạm vi nhiệt độ khá hẹp.
Cách thức hoạt động của enzyme
Hầu hết các enzyme hoạt động bằng cách hạ thấp năng lương̣̣ kich hoaṭ của một phản ứng hóa học. Đôi khi, hình dạng của chúng mang lại cho các chất phản ứng gần nhau về mặt thể chất theo phong cách, có lẽ, của một huấn luyện viên đội thể thao hoặc quản lý nhóm làm việc có ý định hoàn thành nhiệm vụ nhanh hơn. Người ta tin rằng khi các enzyme liên kết với chất phản ứng, hình dạng của chúng thay đổi theo cách làm mất ổn định chất phản ứng và khiến nó dễ bị ảnh hưởng bởi bất kỳ thay đổi hóa học nào trong phản ứng.
Các phản ứng có thể tiến hành mà không cần đầu vào của năng lượng được gọi là phản ứng tỏa nhiệt. Trong các phản ứng này, các sản phẩm hoặc hóa chất được hình thành trong phản ứng có mức năng lượng thấp hơn các hóa chất đóng vai trò là thành phần của phản ứng. Theo cách này, các phân tử, như nước, "tìm kiếm" mức (năng lượng) của chính chúng; các nguyên tử "thích" được sắp xếp với tổng năng lượng thấp hơn, giống như nước chảy xuống đến điểm vật lý thấp nhất có sẵn. Đặt tất cả những điều này lại với nhau, rõ ràng là các phản ứng tỏa nhiệt luôn diễn ra tự nhiên.
Tuy nhiên, thực tế là một phản ứng sẽ xảy ra ngay cả khi không có đầu vào không nói gì về tốc độ xảy ra. Nếu một chất được đưa vào cơ thể sẽ tự nhiên biến thành hai chất dẫn xuất có thể đóng vai trò là nguồn năng lượng trực tiếp của tế bào, điều này sẽ không tốt nếu phản ứng tự nhiên mất nhiều giờ hoặc nhiều ngày để hoàn thành. Ngoài ra, ngay cả khi tổng năng lượng của sản phẩm cao hơn năng lượng của các chất phản ứng, đường năng lượng không phải là độ dốc xuống dốc trơn tru trên biểu đồ; thay vào đó, các sản phẩm phải đạt được mức năng lượng cao hơn mức mà chúng đã bắt đầu để chúng có thể "vượt qua cái bướu" và phản ứng có thể tiến hành. Khoản đầu tư ban đầu này của năng lượng vào các chất phản ứng trả hết dưới dạng sản phẩm đã được đề cập ở trên năng lượng kích hoạthoặc Emột.
Các loại enzyme
Cơ thể con người bao gồm sáu nhóm chính, hoặc các lớp, của các enzyme.
Oxidoreductase tăng cường tốc độ phản ứng oxy hóa và khử. Trong các phản ứng này, còn được gọi là phản ứng oxi hóa khử, một trong những chất phản ứng từ bỏ một cặp electron mà chất phản ứng khác thu được. Các nhà tài trợ cặp electron được cho là bị oxy hóa và hoạt động như một chất khử, trong khi người nhận cặp electron bị giảm được gọi là tác nhân oxy hóa. Một cách đơn giản hơn để đặt điều này là trong các loại phản ứng này, các nguyên tử oxy, nguyên tử hydro hoặc cả hai đều được di chuyển. Các ví dụ bao gồm cytochrom oxydase và lactate dehydrogenase.
Chuyển nhượng tốc độ trong quá trình chuyển các nhóm nguyên tử, chẳng hạn như methyl (CH3), acetyl (CH3CO) hoặc amino (NH2) các nhóm, từ một phân tử đến một phân tử khác. Acetate kinase và alanine deaminase là ví dụ của transferase.
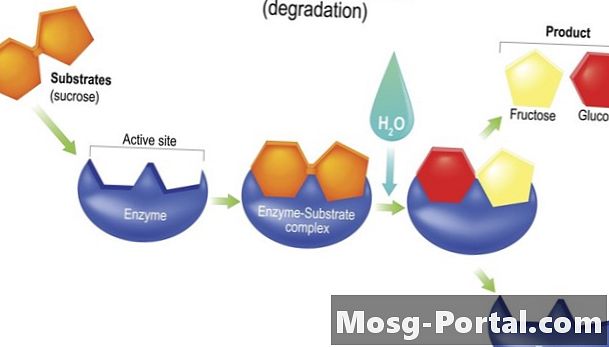
Thủy phân đẩy nhanh phản ứng thủy phân. Phản ứng thủy phân sử dụng nước (H2O) để tách một liên kết trong một phân tử để tạo ra hai sản phẩm con, thường bằng cách gắn -OH (nhóm hydroxyl) từ nước vào một trong các sản phẩm và một -H (nguyên tử hydro) với nhau. Trong khi đó, một phân tử mới được hình thành từ các nguyên tử bị thay thế bởi các thành phần -H và -OH. Các enzyme tiêu hóa lipase và sucrase là hydrolase.
Lyase tăng cường tốc độ bổ sung một nhóm phân tử vào liên kết đôi hoặc loại bỏ hai nhóm khỏi các nguyên tử gần đó để tạo liên kết đôi. Chúng hoạt động giống như thủy phân, ngoại trừ thành phần bị loại bỏ không bị dịch chuyển bởi nước hoặc các phần nước. Lớp enzyme này bao gồm oxalate decarboxylase và isocitrate lyase.
Đồng phân tăng tốc độ phản ứng đồng phân hóa. Đây là những phản ứng trong đó tất cả các nguyên tử ban đầu trong chất phản ứng được giữ lại, nhưng được sắp xếp lại để tạo thành đồng phân của chất phản ứng. (Đồng phân là các phân tử có cùng công thức hóa học, nhưng cách sắp xếp khác nhau.) Ví dụ bao gồm glucose-phosphate isomerase và alanine racemase.
Dây chằng (còn được gọi là synthetase) tăng cường tốc độ nối của hai phân tử. Họ thường thực hiện điều này bằng cách sử dụng năng lượng có được từ sự phân hủy của adenosine triphosphate (ATP). Ví dụ về ligase bao gồm acetyl-CoA synthetase và DNA ligase.
Ức chế enzyme
Ngoài sự thay đổi nhiệt độ và pH, các yếu tố khác có thể dẫn đến hoạt động của enzyme bị giảm hoặc ngừng hoạt động. Trong một quá trình gọi là tương tác allosteric, hình dạng của enzyme tạm thời bị thay đổi khi một phân tử liên kết với một phần của nó cách xa nơi nó tham gia chất phản ứng. Điều này dẫn đến mất chức năng. Đôi khi điều này hữu ích khi bản thân sản phẩm đóng vai trò là chất ức chế allosteric, bởi vì đây thường là dấu hiệu của phản ứng đã tiến hành đến điểm không cần thêm sản phẩm.
Trong ức chế cạnh tranh, một chất gọi là hợp chất điều tiết cạnh tranh với chất phản ứng cho vị trí gắn kết. Điều này giống như cố gắng đặt một số phím làm việc vào cùng một khóa cùng một lúc. Nếu đủ các hợp chất điều hòa này tham gia với một lượng enzyme đủ cao, nó sẽ làm chậm hoặc tắt quá trình phản ứng. Điều này có thể hữu ích trong dược lý bởi vì các nhà vi trùng học có thể thiết kế các hợp chất cạnh tranh với các vị trí gắn kết của các enzyme vi khuẩn, khiến vi khuẩn khó gây bệnh hơn hoặc tồn tại trong cơ thể con người.
Trong ức chế không cạnh tranh, một phân tử ức chế liên kết với enzyme tại một điểm khác với vị trí hoạt động, tương tự như những gì xảy ra trong một tương tác allosteric. Sự ức chế không thể đảo ngược xảy ra khi chất ức chế liên kết vĩnh viễn hoặc làm suy giảm đáng kể enzyme để chức năng của nó không thể phục hồi. Khí thần kinh và penicillin đều sử dụng loại ức chế này, mặc dù với ý định ồ ạt khác nhau trong tâm trí.